第3节 电镀的反应机理
1 电化学反应
下图是电镀装置示意图,被镀的零件为阴极,与直流电源的负极相连,金属阳极与直流电源的正极联结,阳极与阴均浸入镀液中。当在阴阳两极间施加一定电位时,则在阴极发生如下反应:从镀液内部扩散到电极和镀液界面的金属离子Mn+从阴极上获得n个电子,还原成金属M另一方面,在阳极则发生与阴极完全相反的反应,即阳极界面上发生金属M的溶解,释放n个电子生成金属离子Mn+。
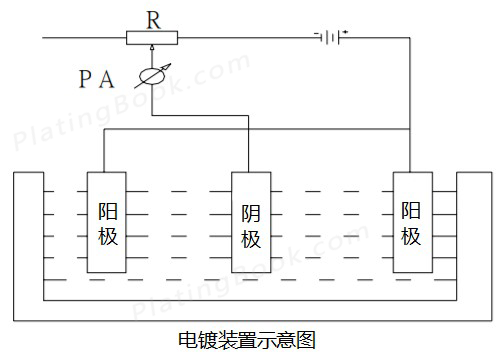
2 法拉第定律
电流通过镀液时,电解质溶液发生电解反应,阴极上不断有金属析出,阳极金属不断溶解。因此,金属的析出(或溶解)量必定与通过的电荷有关。根据大量实验结果,法拉第建立了析出(或溶解)的物质与电荷之间的关系的定律。
2.1 法拉第一定律
电极上析出(或溶解)物质的重量与进行电解反应时所通过的电荷成正比,即:m电极上析出(或溶解)物质的重量与进行电解反应时所通过的电荷成正比,即:
$$ m = kq = kIt $$
式中:
m ------ 为电极上析出或溶解物质的质量;
q ------- 为通过的电荷时;
k ------- 为比例常数;
I ------- 为电流;
t ------- 为通电时间。
2.2 法拉第第二定律
在不同的电解液中,通过相同的电荷量时,在电极上析出(或溶解)物的物质的量相等,并且析出(或溶解)1mol 的任何物质所需的电荷量都是 9.65×104C。这一常数称为法拉第常数,用F表示:
$$ K = \frac{M}{F} $$
3 电流效率
电镀时,阴极上实际析出的物质的质量并不等于根据法拉定律得到的计算结果,实际值总小于计算值,这是由于电极上的反应不只一个,例如镀镍时,在阴极上除发生这一主反应外,还会发生副反应。
4 电镀液的分散能力
镀溶液的分散能力是指电镀液所具有的使金属层厚度均匀分布的能力,也称均镀能力。电镀液的分散能力越好,在不同阴极部位所沉积出的金属层厚度越均匀。
5 电镀液的覆盖能力
在电镀生产中,常用到的另一个概念是覆盖能力,亦称深镀能力,它是指电镀液所具有的使镀件的深凹处沉积上金属镀层的能力。分散能力和覆盖能力不同,前者是说明金属在阴极表面分布均匀程度的问题,它的前提是在阴极表面都有镀层:而后者是指金属在阴极表面的深凹处有无沉积层的问题。
6 电极电位
当金属电极浸入含有该金属离子的溶液中时,存在如下的平衡,即金属失电子而溶解于溶液的反应和金属离子得电子而析出金属的逆反应应同时存在:
$$ M^{n+} + ne ⇋ M $$
平衡电位与金属的本性和溶液的温度,浓度有关。为了精确比较物质本性对平衡电位的影响,人们规定当溶液温度为25℃,金属离子的浓度为1mol/L时,测得的电位叫标准电极电位。标准电极电位负值较大的金属都易失掉电子被氧化,而标准电极电位正值较大的金属都易得到电子被还原。
7 极化
所谓极化就是指有电流通过电极时,电极电位偏离平衡电极电位的现象。所以,又把电流-电位曲线称为极化曲线。产生极化作用的原因主要是电化学极化和浓差极化。
7.1 电化学极化
由于阴极上电化学反应速度小于外电源供给电子的速度,从而使电极电位向负的方向移动而引起的极化作用。
7.2 浓差极化
由于邻近电极表液层的浓度与溶液主体的浓度发生差异而产生的极化称浓差极化,这是由于溶液中离子扩散速度小于电子运动造成的。




